You have successfully logged out.
Otwórz nowe przestrzenie dla implantacji
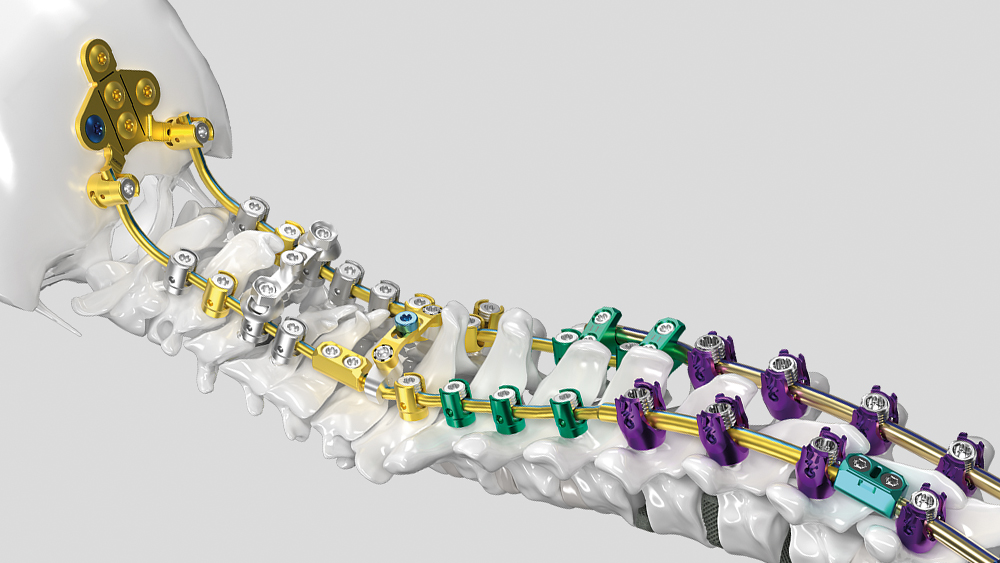
Implanty do stabilizacji międzytrzonowej AESCULAP® 3D
Zainspirowane anatomią człowieka, wspierane przez naukę – nasze klatki (cages) łączą osiągnięcia technologiczne z wartościami klinicznymi. Efektem jest znaczący postęp w stabilizacji przedniej i tylnej.
Jesteś osobą wykonującą zawód medyczny lub prowadzącym obrót wyrobami medycznymi?
Zgodnie z obowiązującymi przepisami prawa, oświadczam, że jestem osobą wykonującą zawód medyczny lub prowadzącym obrót wyrobami medycznymi. Mam świadomość, że treści zamieszczane na niniejszej stronie mogą zawierać między innymi wiadomości na temat wyrobów niebezpiecznych dla zdrowia i bezpieczeństwa pacjentów.
Potwierdź Jestem profesjonalistą z branży medycznej. Anuluj Nie jestem profesjonalistą z branży medycznej.Structan®
Otwiera nowe przestrzenie, dosłownie
Myślisz, że to zwykła struktura implantu? Cóż, pozwól się zaskoczyć nauce kryjącej się za Structan®. Dziesiątki lat doświadczeń w połączeniu z nowoczesną technologią doprowadziły do stworzenia tej struktury - zaprojektowanej z myślą o lepszych wynikach klinicznych i zaawansowanej wydajności biomechanicznej.
-
Powierzchnia jest powiększona
0
-krotnie co zapewnia więcej możliwości dla zrostu kostnego.
-
Mocny i elastyczny jednocześnie – Structan® jest o
0%
bliższy modułowi sprężystości kości korowej. (1-4) *
-
Stabilizacja tylna tylko w
0
modułowej platformie kręgosłupa, która precyzyjnie dostosowuje się do Twoich potrzeb.
Makrosieć
Precyzyjnie wyważona chropowatość powierzchni ma pozytywny wpływ na adhezję osteoblastów. Porowatość odpowiada anatomii człowieka, co tworzy solidną podstawę dla w zrostu kostnego, a tym samym zespolenia z Structan®. [5-8]
/
Mikrostruktura
Znaczne zróżnicowanie osteoblastów i lepsza osteointegracja - w oparciu o dowody naukowe, nasze klatki AESCULAP® 3D Cages odzwierciedlają biologiczne atrybuty struktury beleczkowej, wspomagając zrost kostny.[9-15]
/
Większa przestrzeń
Inteligentnie zaprojektowane klatki wspierające osteointergrację między kością, a implantem - z lub bez substytutu kostnego.
/
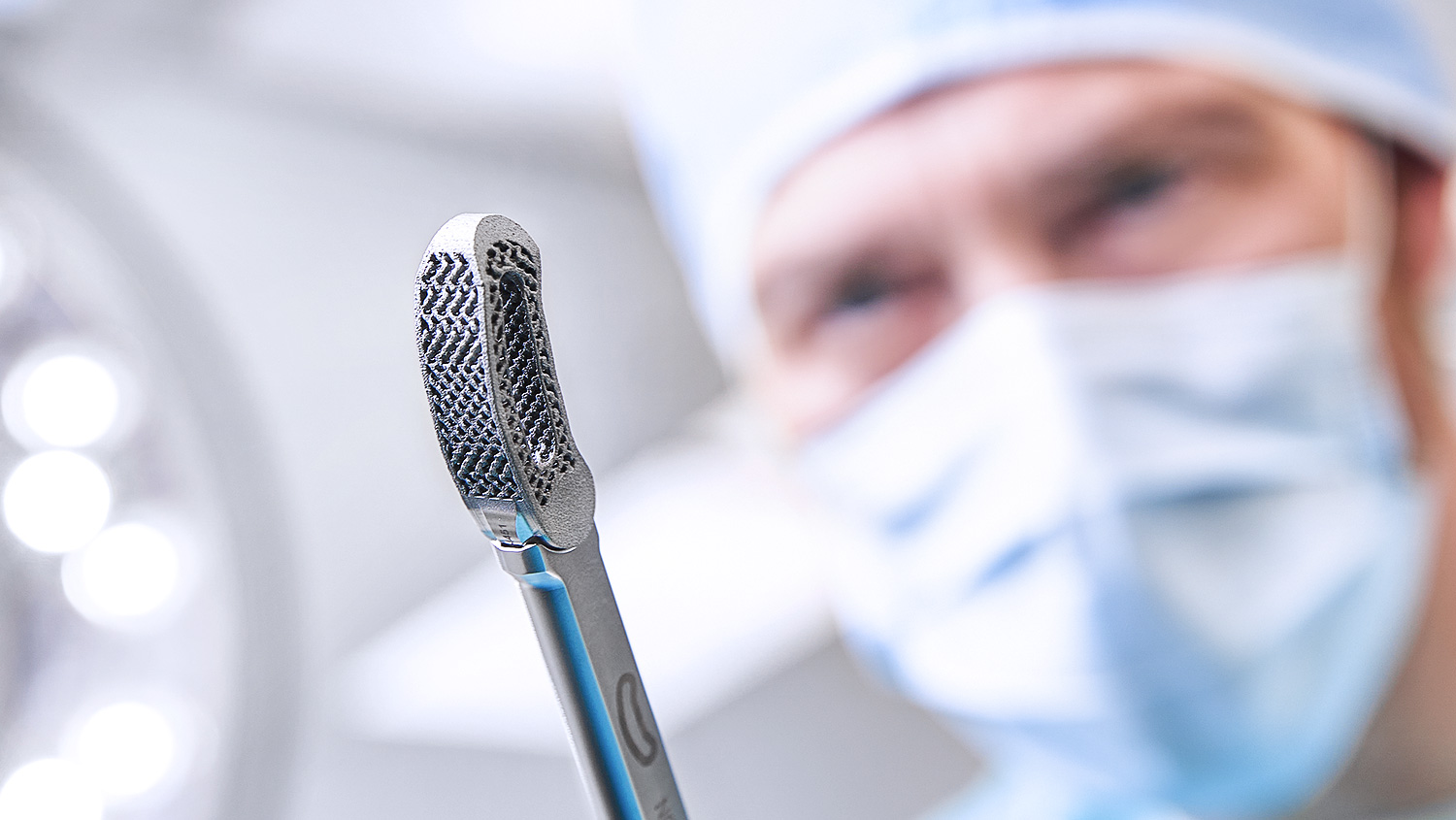
Inteligentny interfejs
Zharmonizowany interfejs zapewnia solidne połączenie z narzędziami i wysoką precyzję podczas użytkowania. Poczuj to wszystko dzięki naszemu inserterowi w procedurach TLIF - ponieważ pewność zapewnia spokój ducha.
/
Implanty do stabilizacji międzytrzonowej AESCULAP® 3D
Zaprojektowane i wyprodukowane w Niemczech
Podobnie jak w przypadku wszystkich naszych rozwiązań dla kręgosłupa, projekt narzędzi do implantacji międzytrzonowej AESCULAP® 3D opiera się na naszych podstawowych wartościach zapewnienia zaawansowanej wydajności biomechanicznej, elastyczności śródoperacyjnej i poprawy wyników klinicznych.
Produkcja przyrostowa
Technologia, która poprawia wyniki kliniczne
Nowe technologie otwierają nowe możliwości rozwoju i produkcji zaawansowanych rozwiązań dla kręgosłupa. Produkcja synergii pozwala nam stworzyć biomechaniczną konstrukcję implantu, która pozytywnie wpływa na zespolenie kostne i dodatkowo poprawia wyniki kliniczne. [16]
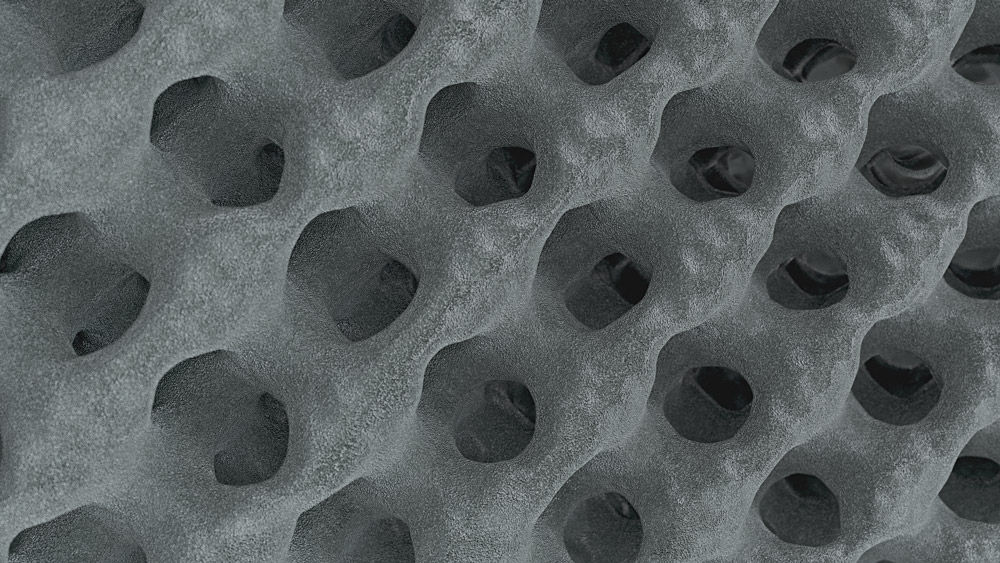
Structan®
Zaawansowana wydajność
Połączenie doskonale wyważonej makrosieci, mikrostruktury i czynników biomechanicznych wyzwala nowe wartości kliniczne w opiece nad pacjentem. Poza poprawą wydajności w zakresie osteointegracji, Structan® zapewnia wyraźną wizualizację bez zakłócających artefaktów co z kolei pozwala dokładnie ocenić pozycję implantu, stan wrastania kości i otaczające struktury kręgosłupa. [17-18]
Portfolio
Implanty do stabilizacji międzytrzonowej AESCULAP® 3D
Od kręgosłupa szyjnego po piersiowo-lędźwiowy, implanty do stabilizacji międzytrzonowej AESCULAP® 3D uzupełniają koncepcje leczenia w zakresie stabilizacji przedniej i tylnej.
Animacje przebiegu zabiegów chirurgicznych
Nasze platformy tworzą prawdziwą synergię
Przyjrzyj się wydajności implantów i narzędzi do stabilizacji międzytrzonowej AESCULAP® 3D i Ennovate®.
TSPACE® 3D z Ennovate®
Nasze instrumentarium do stabilizacji międzytrzonowej TLIF, z inserterem, umożliwia przeprowadzanie prawdziwie minimalnie inwazyjnych procedur stabilizacji.
PROSPACE® 3D z Ennovate®
Dzięki usprawnionej technice chirurgicznej, klatki PLIF i Ennovate® są idealne do zastosowania w technice otwartej.
PROSPACE® Oblique 3D z Ennovate®
Łącząc istotę dwóch światów – nasz TLIF może być wszczepiany z zastosowaniem metody minimalnie inwazyjnej, jak i otwartej.
Odkryj platformę kręgosłupową AESCULAP®
Zaprojektowana z myślą o Twoich potrzebach
Jesteś zainteresowany naszymi implantami AESCULAP® 3D?
Skontaktuj się z nami*compared to solid titanium alloy interbody fusion devices.
[1] Kuhn JL, Goldstein SA, Choi K, London M, Feldkamp LA, Matthews LS. Comparison of the trabecular and cortical tissue moduli from human iliac crests. J Orthop Res. 1989;7(6):876 84.
[2] Ratner BD, Hoffmann AS, Schoen FJ, Lemons JE. An Introduction to Materials in Medicine. Academic Press. 1996.
[3] Chen Y, Wang X, Lu X, Yang L, Yang H, Yuan W, et al. Comparison of titanium and polyetheretherketone (PEEK) cages in the surgical treatment of multilevel cervical spondylotic myelopathy: a prospective, randomized, control study with over 7 year follow up. Eur Spine J. 2013;22(7):1539 46.
[4] Brizuela A, et al. Influence of the elastic modulus on the Osseointegration of Dental Implants. Materials. 2019;12(6):980.
[5] Bostrom M, Boskey A, Kaufman J, Einhorn T. Form and function of bone. In: Orthopaedic Basic Science Biology and Mechanics of the Musculoskeletal System. 2nd ed. Rosemont, IL: AAOS; 2000: 320-369.
[6] Olivares-Navarrete R, Gittens RA, Schneider JM, et al. Rough titanium alloys regulate osteoblast production of angiogenic factors. Spine J 2012; 12:265-272.
[7] Lincks, J. et al. Response of MG63 osteoblast-like cells to titanium and titanium alloy is dependent on surface roughness and composition. Biomaterials 19, 1998. Pages 2219-32.
[8] Elias CN, et al. Mechanical and clinical properties of titanium and titanium based alloys ( Ti G2, Ti G4 cold worked nanostructured and Ti G5) for biomedical applications. Journal of Materials Research and Technology. 2019;8(1):1060 9.
[9] Cheng A, Cohen D, Boyan B et al. Laser-Sintered Constructs with Bio-inspired Porosity and Surface Micro/ Nano-Roughness Enhance Mesenchymal Stem Cell Differentiation and Matrix Mineralization In Vitro. Calcif Tissue Int 2016; 99:625–637.
[10] Wu S-H, Li Y, Zang Y-Q, et al. Porous Titanium-6 Aluminum-4 Vanadium Cage Has Better Osseointegration and Less Micromotion Than a Poly-Ether-Ether-Ketone Cage in Sheep Vertebral Fusion. Art Organs 2013; 37:191-201
[11] Taniguchi N, Fujibayashi S, Takemoto M, Sasaki K, Otsuki B, Nakamura T, Matsushita T, Kokubo T, Matsuda S. Effect of pore size on bone ingrowth into porous titanium implants fabricated by additive manufacturing: An in vivo experiment. Materials Science and Engineering 2016; C59: 690–701.
[12] Changhui Song, Lisha Liu, Zhengtai Deng, Haoyang Lei, Fuzhen Yuan, Yongqiang Yang, Yueyue Li, Jiakuo Yu. Research progress on the design and performance of porous titanium alloy bone implants. Journal of Materials Research and Technology, Volume 23, 2023. Pages 2626-2641, ISSN 2238-7854.
[13] Fukuda A, Takemoto M, Saito T, et al. Osteoinduction of porous Ti implants with a channel structure fabricated by Selective Laser Melting. Acta Biomat 2011; 7:2327-2336.
[14] Ran Q, Yang W, Hu Y, Shen X, Yu Y, Xiang Y, Cai K. Osteogenesis of 3D printed porous Ti6Al4V implants with different pore sizes. J Mech Behav Biomed Mater. 2018 Aug;84:1-11. doi: 10.1016/j.jmbbm.2018.04.010. Epub 2018 Apr 18. PMID: 29709846.
[15] Van Bael S, Chai YC, Truscello S, Moesen M, Kerckhofs G, Van Oosterwyck H, Kruth JP, Schrooten J. The effect of pore geometry on the in vitro biological behavior of human periosteum-derived cells seeded on selective laser-melted Ti6Al4V bone scaffolds. Acta Biomater. 2012 Jul;8(7):2824-34. doi: 10.1016/j.actbio.2012.04.001. Epub 2012 Apr 7. PMID: 22487930.
[16] Kia, C.; Antonacci, C.L.; Wellington, I.; Makanji, H.S.; Esmende, S.M. Spinal Implant Osseointegration and the Role of 3D Printing: An Analysis and Review of the Literature. Bioengineering 2022, 9, 108. https://doi.org/10.3390/bioengineering9030108.
[17] Usability-Test, Usability Validation of AESCULAP® CeSPACE® 3D Cages, Tübingen, 2019.The usability of the AESCULAP® 3D Cage System CeSPACE® 3D was tested in April 2019, in a cadaver workshop with six independent test persons as intended users (surgeons specialized in spinal surgery or comparable fields). Parameters such as implant visibility under x-ray control, mechanical stability of the implant/instrument interface andimplant surface evaluation in terms of tissue injury risk were tested among others. Acceptance criteria were fulfilled for all the above-mentioned parameters. All test users confirmed the absence of critical features that must be improved prior to clinical use. During the test, the x-ray visibility of the cages was particularly positively assessed.
[18] Rehnitz, Christoph, PD Dr. med. Radiological image evaluation of AESCULAP® interbody fusion devices, Heidelberg, 2019. CT and X-ray visualization of different AESCULAP® interbody fusion cages (full titanium, porous Ti6Al4V and PLASMAPOREXP® cages) was tested in a cadaver setup. A radiologist evaluated the implant visibility and the presence of artefacts that may limit the visualization of adjacent structures. Visualization and assessment of implant position was achieved in X-ray and CT for all tested cages. Minor artefacts were visible in CT reconstructions in the surrounding of porous Ti6Al4V and full titanium implants. Porous Ti6Al4V implants showed slightly fewer artefacts in CT in comparison to full titanium implants. The minor artefacts observed did not limit the assessment of the surrounding anatomical structures.